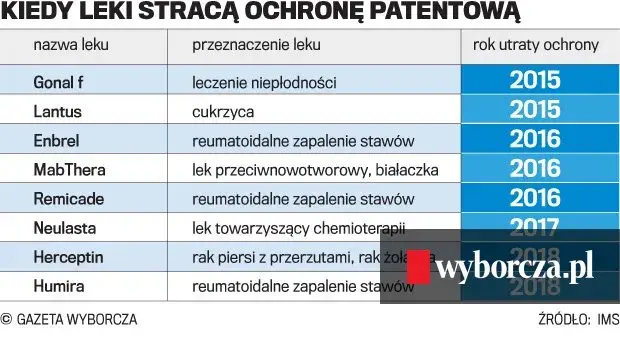
Zrozumienie mechanizmów ochrony patentowej leków w Polsce jest niezwykle istotne, ponieważ wpływa na dostępność innowacyjnych terapii, koszty leczenia oraz rozwój przemysłu farmaceutycznego. Jako ekspertka w tej dziedzinie, często spotykam się z pytaniami dotyczącymi tego, jak długo lek jest chroniony i co dzieje się po wygaśnięciu tej ochrony. W tym artykule wyjaśnię kluczowe aspekty prawne, w tym podstawowy okres patentowy, rolę Dodatkowych Praw Ochronnych (SPC) oraz konsekwencje pojawienia się leków generycznych na rynku.
Ochrona patentowa leków w Polsce trwa 20 lat, z możliwością przedłużenia do 15 lat realnej wyłączności rynkowej
- Podstawowy okres ochrony patentowej na lek (substancję czynną) wynosi 20 lat od daty zgłoszenia w Urzędzie Patentowym.
- Faktyczna wyłączność rynkowa jest często krótsza z powodu długotrwałych procedur rejestracyjnych.
- Dodatkowe Prawo Ochronne (SPC) może przedłużyć ochronę o maksymalnie 5 lat, rekompensując czas potrzebny na uzyskanie pozwolenia na dopuszczenie do obrotu.
- Całkowity okres ochrony rynkowej (patent + SPC) nie może przekroczyć 15 lat od momentu uzyskania pierwszego pozwolenia na dopuszczenie do obrotu.
- Badania pediatryczne mogą dodatkowo wydłużyć SPC o 6 miesięcy.
- Po wygaśnięciu ochrony patentowej i SPC na rynek wchodzą tańsze leki generyczne, zwiększając dostępność terapii.

Podstawowa ochrona patentowa leków: 20 lat od zgłoszenia
W Polsce, zgodnie z ustawą Prawo własności przemysłowej, patent na wynalazek, w tym na nową substancję czynną leku, jest przyznawany na okres 20 lat. Ten czas liczy się od daty dokonania zgłoszenia wynalazku w Urzędzie Patentowym Rzeczypospolitej Polskiej. Jest to standardowy i niezmienny okres, który ma na celu zapewnienie wynalazcom wyłączności na ich innowacje.
Co dokładnie chroni patent na lek: substancja czynna czy gotowy produkt?
Kiedy mówimy o patencie na lek, musimy pamiętać, że zasadniczo chroni on substancję czynną, czyli innowacyjną molekułę odpowiedzialną za działanie terapeutyczne. Patent niekoniecznie obejmuje gotowy produkt farmaceutyczny w jego finalnej formie, z jego konkretnym opakowaniem czy dawką. To właśnie odkrycie i rozwój nowej, unikalnej substancji czynnej jest sercem wynalazku i zasługuje na ochronę.
Od kiedy liczy się bieg 20-letniego okresu ochronnego?
To bardzo ważne, aby zrozumieć, że 20-letni okres ochronny liczy się od daty dokonania zgłoszenia patentowego w Urzędzie Patentowym, a nie od momentu wprowadzenia leku na rynek czy rozpoczęcia jego sprzedaży. Jest to kluczowa informacja, która często bywa mylona, a ma fundamentalne znaczenie dla faktycznego czasu wyłączności rynkowej.
Dlaczego realna ochrona rynkowa jest często znacznie krótsza niż 20 lat?
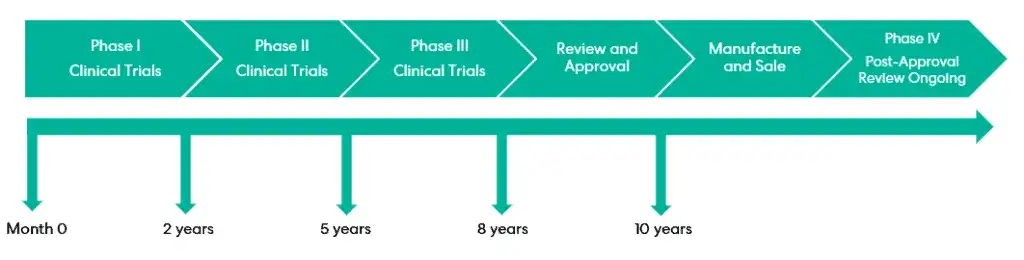
Mimo że patent trwa 20 lat, faktyczny czas, w którym lek jest chroniony na rynku i generuje wyłączny zysk dla producenta, jest zazwyczaj znacznie krótszy. Wynika to z konieczności prowadzenia długotrwałych i kosztownych badań klinicznych, a także skomplikowanych i czasochłonnych procedur rejestracyjnych, zanim lek uzyska pozwolenie na dopuszczenie do obrotu. Te etapy mogą pochłonąć nawet 10-12 lat z 20-letniego okresu patentowego, co znacząco skraca czas realnej wyłączności rynkowej.
Dodatkowe Prawo Ochronne (SPC): Jak przedłużyć monopol rynkowy?
Aby zrekompensować firmom farmaceutycznym ten utracony czas, który jest niezbędny na badania i rejestrację, wprowadzono mechanizm Dodatkowego Prawa Ochronnego (SPC Supplementary Protection Certificate). Jest to swego rodzaju przedłużenie ochrony patentowej, specyficzne dla produktów leczniczych i produktów ochrony roślin. Moim zdaniem, SPC jest kluczowe dla utrzymania innowacyjności w branży farmaceutycznej, ponieważ zachęca firmy do inwestowania w rozwój nowych leków, dając im szansę na odzyskanie poniesionych nakładów.
Jakie warunki musi spełnić lek, aby uzyskać ochronę w ramach SPC?
- Produkt leczniczy musi być chroniony podstawowym patentem, który jest w mocy.
- Musi być uzyskane ważne pozwolenie na dopuszczenie do obrotu dla tego produktu leczniczego w Unii Europejskiej.
- Produkt leczniczy nie mógł być wcześniej przedmiotem innego SPC.
- Pozwolenie na dopuszczenie do obrotu musi być pierwszym pozwoleniem na dopuszczenie do obrotu tego produktu leczniczego.
Jak w praktyce oblicza się maksymalny, 5-letni okres trwania SPC?
Okres trwania SPC jest obliczany na podstawie czasu, jaki upłynął między datą zgłoszenia podstawowego patentu a datą uzyskania pierwszego pozwolenia na dopuszczenie do obrotu w Unii Europejskiej, pomniejszonego o pięć lat. Maksymalny okres trwania SPC wynosi jednak 5 lat. Oznacza to, że nawet jeśli różnica między zgłoszeniem a pozwoleniem na obrót wyniesie np. 12 lat (12 - 5 = 7), SPC i tak zostanie przyznane na maksymalne 5 lat. Jest to mechanizm, który ma zrównoważyć interesy innowatorów z potrzebami rynku.
Czy całkowity czas ochrony patentowej i SPC może przekroczyć 15 lat od wejścia na rynek?
Warto podkreślić, że całkowity okres ochrony rynkowej, obejmujący zarówno podstawowy patent, jak i Dodatkowe Prawo Ochronne (SPC), nie może przekroczyć 15 lat od momentu uzyskania pierwszego pozwolenia na dopuszczenie do obrotu w Unii Europejskiej. Jest to górna granica, która ma zapewnić równowagę między ochroną innowacji a dostępnością leków generycznych.
Dodatkowe pół roku ochrony dzięki badaniom pediatrycznym
System prawny przewiduje również dodatkową zachętę dla firm farmaceutycznych do prowadzenia badań nad lekami dla dzieci. Istnieje możliwość przedłużenia SPC o dodatkowe 6 miesięcy (tzw. przedłużenie pediatryczne). Warunkiem jest przeprowadzenie badań klinicznych produktu leczniczego z udziałem populacji pediatrycznej, zgodnie z zatwierdzonym planem badań pediatrycznych (PIP Paediatric Investigation Plan). Jest to niezwykle ważne, ponieważ dzieci często potrzebują specjalnie dostosowanych dawek i formulacji, a badania w tej grupie wiekowej są szczególnie wymagające.
Czy każda firma farmaceutyczna może ubiegać się o to dodatkowe pół roku?
Tak, każda firma farmaceutyczna, która spełni warunki dotyczące przeprowadzenia badań pediatrycznych i uzyska zatwierdzenie planu PIP, może ubiegać się o to dodatkowe przedłużenie SPC. To zachęta dla wszystkich podmiotów, aby inwestowały w rozwój leków bezpiecznych i skutecznych dla najmłodszych pacjentów.

Koniec wyłączności: Co dzieje się po wygaśnięciu ochrony patentowej?
Wygaśnięcie ochrony patentowej i ewentualnego Dodatkowego Prawa Ochronnego (SPC) to moment przełomowy dla rynku farmaceutycznego. Oznacza to, że drzwi otwierają się dla konkurencji. Producenci leków generycznych mogą wówczas wprowadzać na rynek swoje tańsze odpowiedniki. Warto wspomnieć o mechanizmie "SPC manufacturing waiver", wprowadzonym w 2019 roku, który pozwala firmom z UE na produkcję generyków lub biopodobnych leków w trakcie trwania SPC, ale wyłącznie na eksport poza UE lub w celu magazynowania przez ostatnie 6 miesięcy trwania SPC, aby mogły być wprowadzone na rynek UE natychmiast po jego wygaśnięciu. To strategiczne posunięcie, które ma na celu przyspieszenie dostępności generyków.
Era leków generycznych: Jak wejście konkurencji wpływa na ceny i dostępność terapii?
Po wygaśnięciu wyłączności rynkowej na rynek masowo wchodzą leki generyczne (odtwórcze). Ich pojawienie się ma ogromny wpływ na rynek: ceny leków znacząco spadają, często o kilkadziesiąt procent. To z kolei przekłada się na zwiększoną dostępność terapii dla pacjentów oraz generuje znaczne oszczędności dla budżetów systemów opieki zdrowotnej. Moim zdaniem, jest to jeden z najważniejszych mechanizmów zapewniających powszechny dostęp do skutecznych i bezpiecznych leków.
Lek oryginalny a generyczny: czym się różnią i czy jest się czego obawiać?
Wielu pacjentów zastanawia się nad różnicami między lekiem oryginalnym a generycznym. Kluczowe jest zrozumienie, że leki generyczne zawierają tę samą substancję czynną, w tej samej dawce i formie farmaceutycznej, co ich oryginalne odpowiedniki. Muszą one również wykazać bioekwiwalencję, co oznacza, że działają w organizmie w ten sam sposób i są tak samo bezpieczne i skuteczne. Nie ma więc powodów do obaw lek generyczny to po prostu tańsza wersja sprawdzonej terapii.
Inne mechanizmy ochrony: Wyłączność danych i rynkowa
Poza ochroną patentową i SPC, istnieją inne mechanizmy, które stanowią bariery wejścia na rynek dla leków generycznych. Są to tzw. wyłączność danych (data exclusivity) i wyłączność rynkowa (market exclusivity). Mechanizmy te są niezależne od patentu i mają na celu dalszą ochronę innowacyjnych produktów leczniczych, nawet jeśli patent na substancję czynną już wygasł.
Czym jest wyłączność danych i dlaczego blokuje konkurencję nawet bez patentu?
Wyłączność danych to okres, w którym producent leku generycznego nie może powoływać się na dane przedkliniczne i kliniczne, które zostały złożone przez producenta leku oryginalnego w procesie rejestracji. Oznacza to, że aby wprowadzić generyk na rynek, musiałby przeprowadzić własne, kosztowne i czasochłonne badania, co w praktyce skutecznie blokuje jego wejście na rynek przez ten okres, nawet jeśli patent na substancję czynną już wygasł. Jest to potężna tarcza ochronna dla innowatorów.
Przeczytaj również: Psycholog a recepta: Kto przepisze leki psychotropowe w Polsce?
Wyłączność rynkowa w systemie 8+2+1: Jak działa ta dodatkowa tarcza ochronna?
W Unii Europejskiej obowiązuje system "8+2+1", który szczegółowo reguluje wyłączność danych i rynkową dla nowych produktów leczniczych. Oznacza to:
- 8 lat ochrony danych rejestracyjnych: Przez ten czas producent leku generycznego nie może powoływać się na dane z badań leku oryginalnego.
- 2 lata wyłączności rynkowej: Po upływie 8 lat wyłączności danych, przez kolejne 2 lata lek generyczny nadal nie może zostać wprowadzony na rynek, nawet jeśli dysponuje własnymi danymi lub patent wygasł.
- Potencjalny dodatkowy 1 rok wyłączności rynkowej: Jeśli w ciągu pierwszych 8 lat wyłączności danych, lek oryginalny uzyska nowe, istotne wskazanie terapeutyczne, które przynosi znaczące korzyści kliniczne w porównaniu do istniejących terapii, producent może uzyskać dodatkowy rok wyłączności rynkowej.
Ten system zapewnia kompleksową ochronę, która ma na celu promowanie innowacji, jednocześnie przygotowując rynek na wejście tańszych alternatyw po upływie określonego czasu.